Перелом таранной кости
Введение.
Перелом таранной кости – редкая и сложная патология. Составляет менее 1 % от переломов костей скелета, менее 20% от переломов костей стопы.
Переломы таранной кости можно разделить на переломы шейки, тела, головки и отростков.
Переломы шейки таранной кости встречаются наиболее часто (50%). Являются следствием высокоэнергетической травмы (ДТП, падение с высоты). Механизм травмы – форсированное тыльное сгибание стопы и одновременная осевая нагрузка. Часто сопровождается другими переломами как в области голени так и бедра с той же стороны.
Переломы тела таранной кости – составляют 13-23%, чаще результат высокоэнергетической травмы, осевая нагрузка в положении пронации и супинации стопы.
Переломы головки таранной кости – практически никогда не встречаются в изолированном варианте.
Переломы наружного отростка таранной кости – составляют 10-11% от переломов. Происходят под воздействием осевой нагрузки в положении тыльного сгибания стопы, инверсии и наружной ротации. Часто встречается у сноубордистов.
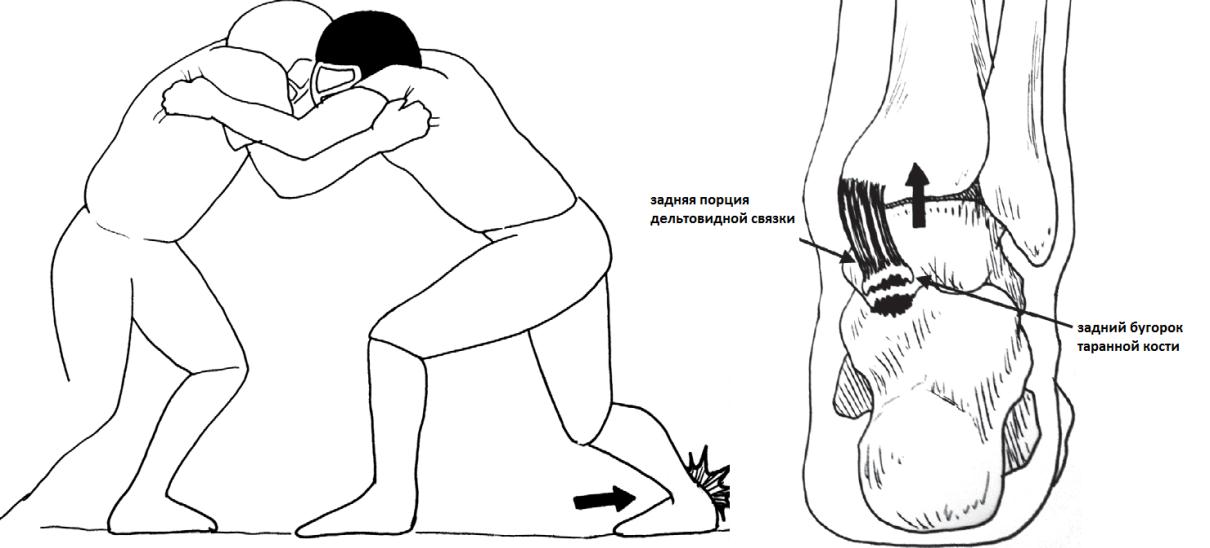
Переломы заднего отростка таранной кости – следствие отрыва фрагмента кости задней большеберцово-таранной связкой, или задней порцией дельтовидной связки. Вторым механизмом травмы часто встречается у спортсменов, особенно футболистов.
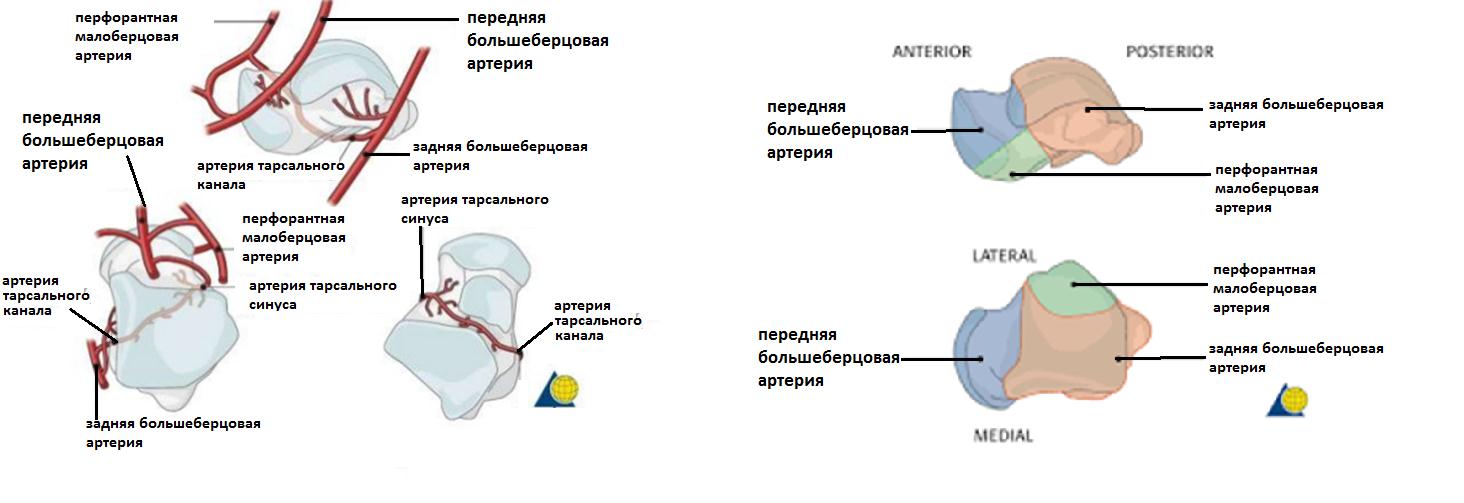
Таранная кость имеет сложную анатомию и небольшое количество источников кровоснабжения, что во многом определяет трудности в лечении её повреждений, и зачастую неудовлетворительные функциональные результаты.
Перелом шейки таранной кости.
Классификации переломов шейки таранной кости Hawkins основана на степени и направлении смещения, что в свою очередь определяет степень нарушения кровоснабжения и риск аваскулярного некроза.
|
Hawkins 1 |
несмещённые |
0-13% риск аваскулярного некроза |
|
|
Hawkins 2 |
Подвывих в подтаранном суставе |
20-50% риск аваскулярного некроза |
|
|
Hawkins 3 |
Подвывих в подтаранном и большеберцово-таранном суставах |
20-100% риск аваскулярного некроза |
|
|
Hawkins 4 |
Полный вывих таранной кости |
70-100% риск аваскулярного некроза |
|
Диагностика перелома шейки таранной кости.
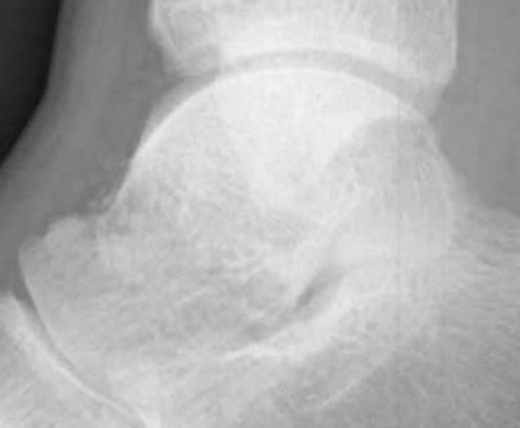
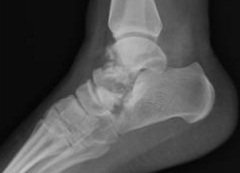
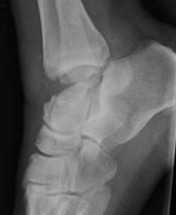
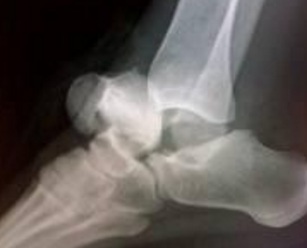
Помимо клинической картины для полноценной диагностики обязательно выполнение рентгенограмм. Помимо прямой и боковой проекции используется Canale проекция, оптимальная для визуализации шейки таранной кости.
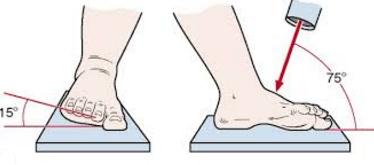
Проекция Canale в максимальном эквинусе, пронация 15 °, снимок под углом 75°.
В затруднительных случаях показано выполнение КТ.
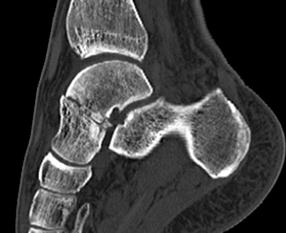
Лечение переломов шейки таранной кости.
В случае острого перелома со смещением во всех случаях показано закрытое устранение смещения. При удовлетворительном положении отломков (смещение менее 2 мм) возможно консервативное лечение, гипсовая иммобилизация 8-12 недель, 6 недель без нагрузки на ногу.
Во всех случаях переломов со смещением показана открытая репозиция и остеосинтез.
Для адекватной визуализации всей шейки таранной кости и контроля качества репозиции рекомендовано использовать 2 доступа, антеромедиальный и антеролатеральный.
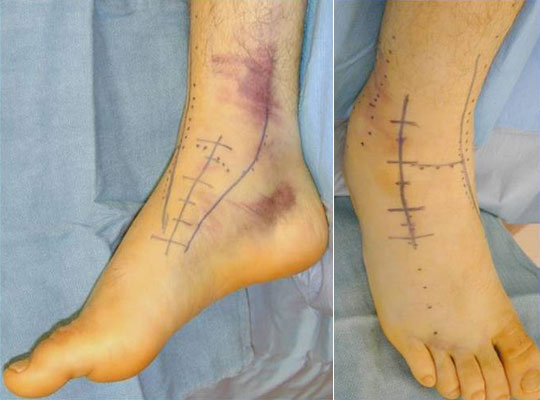
Для удобства выполнения операции желательно наличие дистрактора, джойстиков (винт Шанца + универсальная рукоятка), налобного фонаря для лучшего освещения. В случае затруднений репозиции рекомендуется расширенный доступ через внутреннюю лодыжку.
После достижения репозиции выполняется предварительная фиксация спицами. Часто определяется зона смятия костной ткани по передне-внутренней и передне-наружной поверхности. В этой ситуации показано использование костного трансплантата или синтетического остеозамещающего материала.
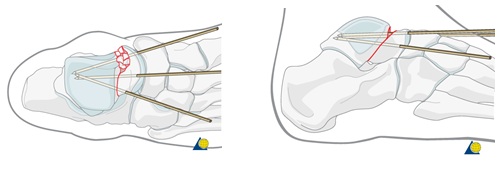
После рентгенологического контроля выполняется окончательная фиксация перелома компрессирующими винтами и\или пластинами и винтами.
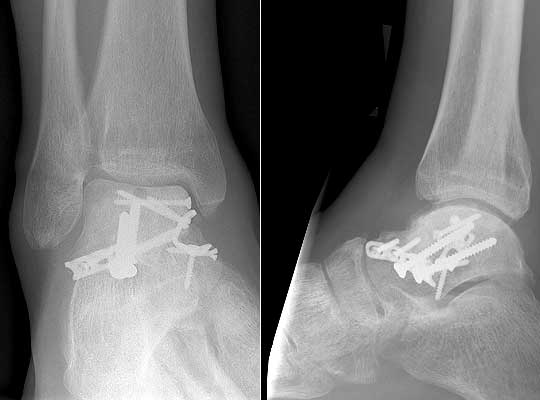
После открытой репозиции и остеосинтеза следует 3 месячный период без нагрузки. Необходимо по возможности предавать конечности возвышенное положение, использовать охлаждение местно. Разработка активных и пассивных движений с первых суток после операции.
К сожалению переломы шейки таранной кости сопровождаются большим количеством осложнений. В 50% случаев развивается подтаранный артроз, в 33%большеберцово-таранный артроз. В зависимости от степени смещения возрастает риск аваскулярного некроза. Его можно выявить по рентгенограммам на 6-8 неделе после операции, в виде очагов склероза, на фоне разрежения костной плотности в области купола таранной кости.
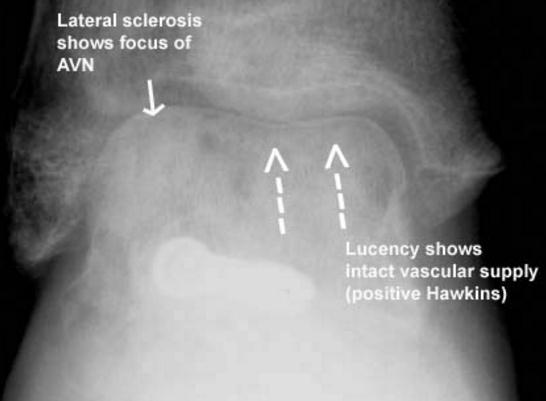
Перелом тела таранной кости
Встречаются более редко чем переломы шейки таранной кости. Принципы лечения остаются прежними – консервативное лечение если смещение составляет менее 2 мм и оперативное если более 2 мм. Для адекватной визуализации тела таранной кости потребуется остеотомия лодыжки (чаще внутренней).
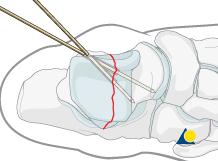
После адекватной репозиции производится предварительная фиксация спицами.
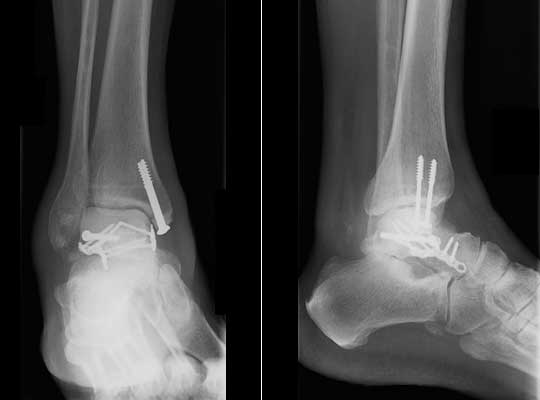
Для окончательной фиксации перелома используются компрессирующие винты диаметром 3,5 и 4 мм, а при необходимости пластины.
Для переломов тела таранной кости свойственны те же осложнения что и для переломов шейки.
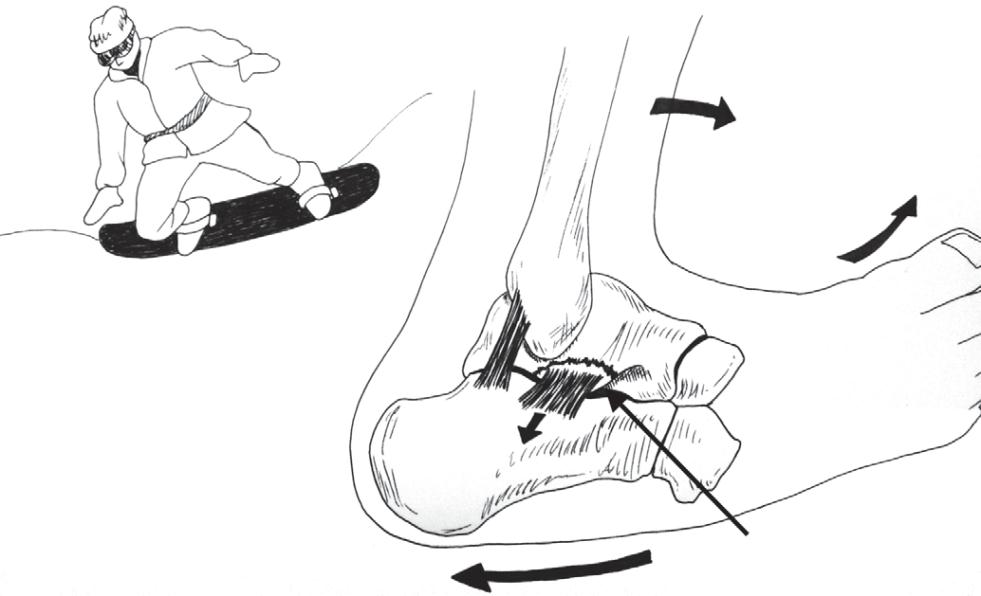
Переломы латерального отростка таранной кости.
Этот перелом часто путают с обычным растяжением связок голеностопа. Механизм повреждения – форсированная эверсия с осевой нагрузкой на задний отдел стопы. Также этот перелом часто называют переломом сноубордиста.
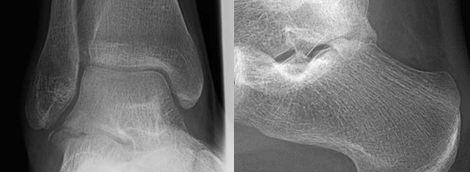
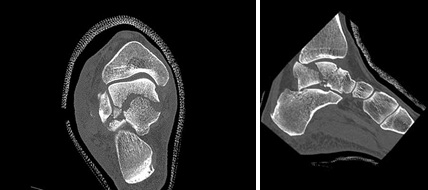
Выявить перелом на обычных прямых рентгенограммах не всегда удаётся. В этой ситуации на выручку приходит КТ.
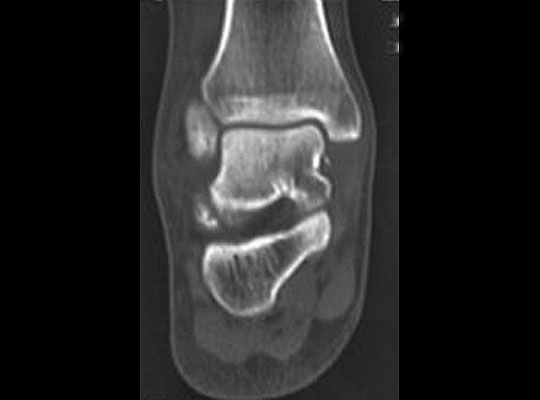
Для переломов латерального отростка таранной кости используется классификация Hawkins.
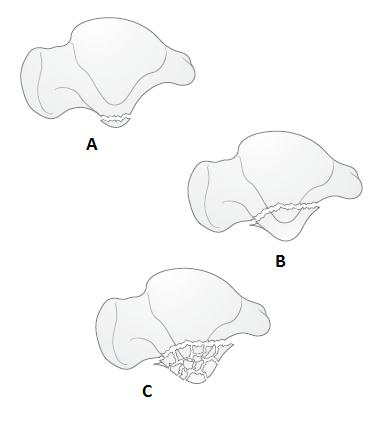
Переломы латерального отростка всегда являются внутрисуставными, так как латеральный отросток учавствует в артикуляции как с пяточной костью, так и с малоберцовой. По этой причине, если перелом со смещением – рекомендуется оперативное лечение. В случае если перелом относится к типу В, то возможно выполнить открытую репозицию и остеосинтез, при переломах типа С, выполняют резекцию латерального отростка. В случае симптомного несращения при застарелых повреждениях также выполняют резекцию.
Для оперативного лечения используют прямой наружный доступ, непосредственно под верхушкой наружной лодыжки. В случае, когда есть возможность выполнить остеосинтез, наружный отросток таранной кости фиксируется одним или двумя винтами, 2,4 или 3,5 мм в зависимости от размера фрагмента. Когда фрагмент слишком мал или раздроблен выполняется его резекция.
Перелом заднего отростка таранной кости.
Для перелома заднего отростка таранной кости характерны несколько различных механизмов возникновения. В зависимости от механизма, отличается и морфология перелома.
Первый механизм – резкое тыльное сгибание в голеностопном суставе. Чаще имеет место у атлетов, либо как результат резкого перехода в положение присяда, либо из-за неудачного приземления после прыжка.
Второй механизм – резкое тыльное сгибание с одновременным давлением на область пяточного бугра.
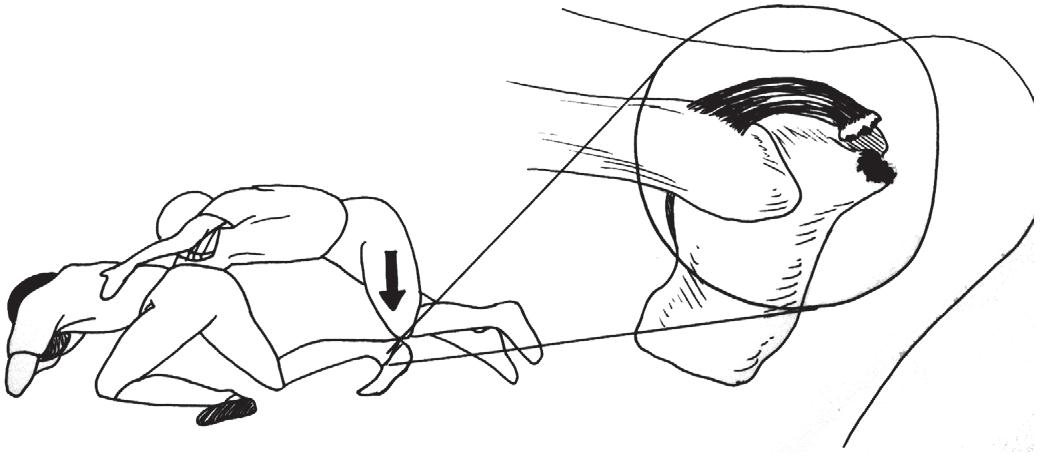
И третий механизм – часто встречающийся у футболистов и танцоров, избыточное тыльное сгибание. Для осуществления этого механизма необходимо наличие анатомически достаточно крупного заднего отростка таранной кости.
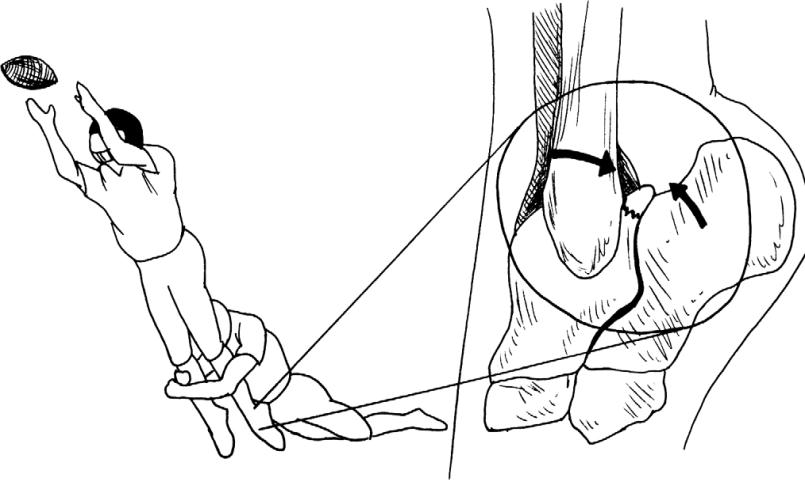
Диагноз перелома заднего отростка таранной кости очень часто ставится несвоевременно или не ставится вообще. Это связано как со смазанной клинической картиной, так и с трудностями визуализации. При клиническом осмотре выполняется тест заднего соударения – большой и указательный пальцы одной руки размещаются параахиллярно и осуществляют давление в направлении заднего отростка таранной кости, при этом другой рукой осуществляется подошвенное сгибание. Если тест вызывает боль, заклинивание, хруст – всё это указывает на повреждение заднего отростка таранной кости. При рентгенограммах часто выявляется треугольная кость, отличающаяся от перелома заднего отростка ровными контурами и округлой формой. Она также зачастую может стать причиной болей по задней поверхности голеностопного сустава, особенно в случае повреждения её синхондроза с задним отростком. В подобных случаях показано её удаление.
При переломах без смещения возможно консервативное лечение, заключающееся в гипсовой иммобилизации сроком на 6 недель. При наличии значимого смещения, крупном отломке – рекомендуется оперативное лечение, открытая репозиция и фиксация 1 или 2 винтами. При оскольчатых или застарелых переломах, сопровождающихся выраженными болями, рекомендуется резекция заднего отростка. В общих чертах лечение проводится по тем же принципам что и для наружного отростка.
Остеохондральные повреждения(остеохондрит) таранной кости.
Что такое остеохондрит таранной кости?
Остеохондральные повреждения таранной кости иногда называемые также остеохондритом, рассекающим остеохондритом или остеохондральными переломами – это повреждения хряща и подлежащих структур купола таранной кости. Остеохондрит таранной кости - одна из причин болей в голеностопном суставе, с которыми пациент обращается к травматологу-ортопеду. Остеохондрит таранной кости часто остаётся нераспознанным и может привести к серьёзным последствиям при отсутствии лечения. Например, остеохондральные повреждения таранной кости встречаются в 40% случаев переломов лодыжек.
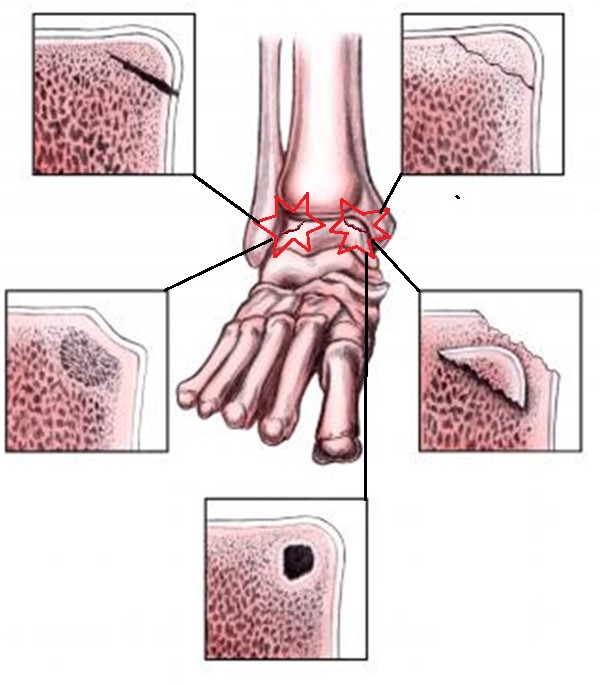
Симптомные остеохондральные повреждения таранной кости часто требуют хирургического вмешательства. Эти повреждения обычно становятся следствием одного или нескольких травматических событий, приводящих к частичному или полному отрыву участка хряща с подлежащей костью. Такие дефекты вызывают глубокую боль в области голеностопного сустава при осевой нагрузке, ограничение амплитуды движения, нарушение функции ходьбы, тугоподвижность, ощущение заклинивания сустава, отёк. Эти симптомы могут стать причиной ограничений физической активности и инвалидизации.
История изучения остеохондрита таранной кости.
Впервые термин «рассекающий остеохондрит» был опубликован Konig в 1888, он описал формирование свободного тела в коленном суставе как следствие перелома суставного хряща и подлежащей кости.
В 1922 Kappis описал это явление в голеностопном суставе. В 1959 коду Berndt и Harty предложили рентгенологическую классификацию этих повреждений, и хотя она значительно видоизменилась за прошедшее с того момента время, она по прежнему широко используется. В настоящее время в сообществе травматологов-ортопедов используется термин остеохондрального повреждения таранной кости (сокращённо ОПТК) как наиболее точно отражающий суть проблемы, которая редко сводится к единичной травме (перелому), аваскулярному некрозу ( рассекающий остеохондрит) или постоянной микротравме, а включает совокупность всех вышеперечисленных факторов.
Анатомичесике исследования проведенные с использованием кадаверного материала показали, что основным механизмом приводящим к остеохондральным переломам наружной части купола таранной кости является её форсированная инверсия. Указание на травму встречается примерно в 85 % случаев ОПТК (Остеохондральных повреждений таранной кости) однако в 15 % случаев пациенты не могут связать появление болей с травматическим событием. Чаще всего это встречается в тех случаях когда очаг повреждения расположен по задне - внутренней поверхности таранной кости. Также встречаются случаи двухсторонних повреждений и одинаковых повреждений наблюдаемых в семьях или у однояйцевых близнецов, что свидетельствует о возможной генетической предрасположенности к аваскулярному некрозу у части пациентов.
Лечебная тактика в отношении ОПТК претерпела значительные изменения за последние 10 лет. Консервативное лечение для лёгких повреждений включает функциональную разгрузку или гипсовую иммобилизацию. Хирургическое лечение предназначено для более серьёзных повреждений и включает иссечение, иссечение и кюретаж, иссечение+кюретаж+микрофрактурирование или рассверливание, установка ауто- или алло-трансплантата, антеградное и ретроградное рассверливание, фиксация фрагмента при помощи биодеградируемых винтов, аутологичная имплантация хондроцитов и некоторые другие. Ниже мы приведём сравнение их эффективности.
Целью лечения остеохондральных повреждений во всех случаях является уменьшение боли, отёка, увеличение амплитуды движений и восстановление функции. Во многих случаях возможно использование нескольких из вышеперечисленных методик, в зависимости от предпочтений хирурга.
Остеохондральные повреждения таранной кости редкое заболевание, однако оно значительно чаще встречается в группе пациентов перенёсших в анамнезе перелом лодыжек или страдающих от нестабильности голеностопного сустава.
Патофизиология остеохондральных повреждений таранной кости.
Передне-наружные ОПТК являются следствием инверсии и тыльного сгибания стопы, для них характерна большая площадь и они редко бывают глубокими. Скорее всего это связано с продольным направлением вектора силы травмы.
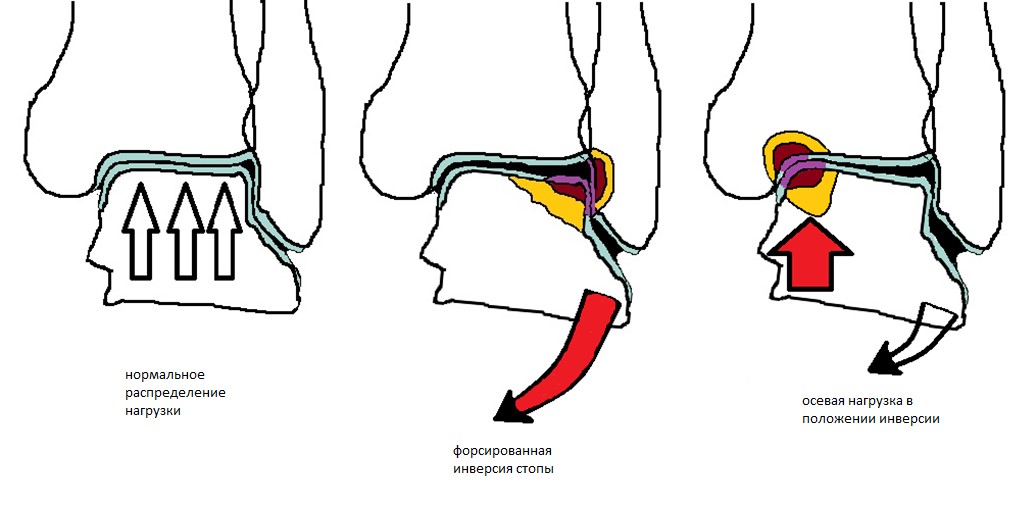
ОПТК по задне – медиальной поверхности, наоборот, чаще бывают глубокими, чашеобразными или сопровождаются формированием кисты с шапочкой из хряща сверху. По видимому это связано с вертикальным концентрированным направлением вектора силы травмы.
Таким образом становится понятно, что остеохондральные повреждения таранной кости часто сочетаются с нестабильностью голеностопного сустава, повреждением связочного аппарата голеностопного сустава, переломами лодыжек.
В анатомических исследованиях было показано что хрящ таранной кости на 18-35 % мягче чем хрящ соответствующих участков большеберцовой кости. Толщина хряща обратно пропорциональна испытываемой им нагрузке, что также может оказывать влияние на локализацию зоны повреждения.
Как показали исследования распределение нагрузки в голеностопном суставе нарушается при размере дефекта более 7,5\15 мм, что может быть использовано с целью прогнозирования отсроченных результатов.
Классификация остеохондральных повреждений таранной кости.
Рентгенологическая классификация остеохондральных повреждений таранной кости Berndt и Harty
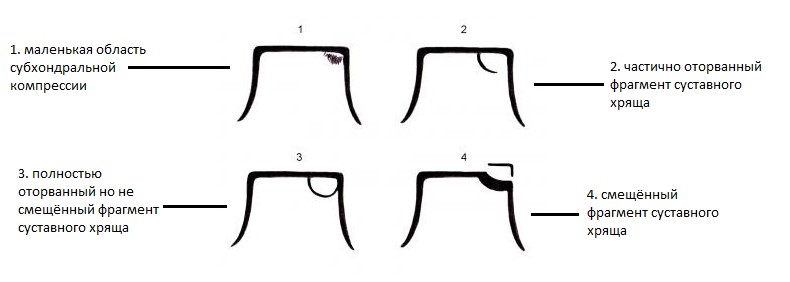
КТ классификация остеохондральных повреждений таранной кости Ferkel и Sgaglione
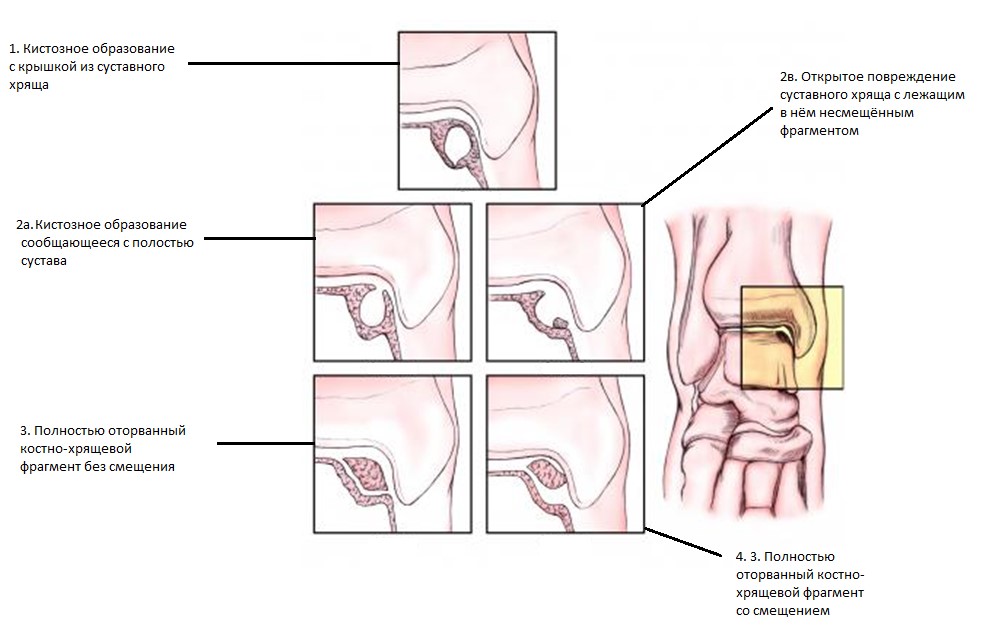
МРТ классификация остеохондральных повреждений таранной кости Hepple.
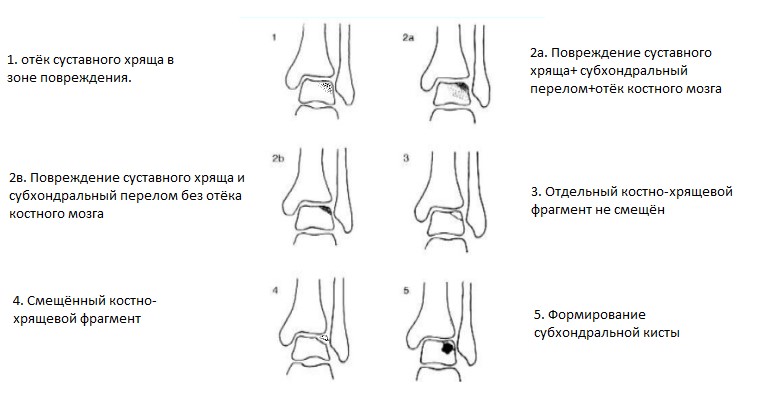
Диагностика остеохондрального повреждения таранной кости.
Диагностика ОПТК сложная задача, часто при первичном обращении ставится диагноз повреждение и перенапряжение капсульно связочного аппарата или ушиб, однако длительно персистирующие боли настораживают травматолога-ортопеда и заставлют двигаться в направлении более информативных методов обследования.
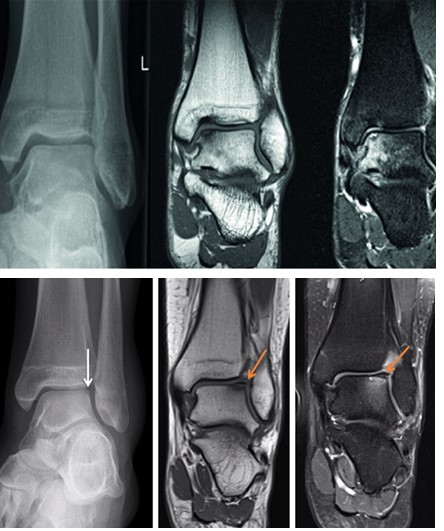
Симптомы остеохондрального повреждения таранной кости.
- Глубокая боль в области голеностопного сустава
- Боль при осевой нагрузке (стоя)
- Боль при ходьбе и беге
- Ограничение амплитуды движений
- Отёк в области голеностопного сустава
- Заклинивание, блоки сустава
Консервативное лечение остеохондральных повреждений таранной кости.
6 недель гипосовой иммобилизации без осевой нагрузки, с последующей ЛФК - при 1-2\2а стадиях заболевания (независимо от системы классификации). Во всех остальных случаях показано оперативное лечение. Эффективность консервативного лечения составляет 45-50%.
Хирургическое лечение остеохондральных повреждений таранной кости.
Хирургическое лечение ОПТК зависит от многих факторов: характеристики пациента такие как возраст, уровень активности, сопутсвующие заболевания, характеристики самого повреждения такие как его расположение, размер, глубина поражения, морфология поражения, длительность. В основном хирургическое лечение опирается на один из трёх принципов: 1) удаление свободного тела с или без стимуляции костного мозга посредством микрофрактурирования, рассверливания 2) сохранение хряща за счёт ретроградного рассверливания, фиксации фрагмента или замещение дефекта губчатой костью 3) стимуляция формирования нового гиалинового хряща за счёт пересадки костно-хрящевого блока, мозаичной хондропластики, аллографта.
Предоперационная подготовка при остеохондральных повреждений таранной кости.
Необходимо тщательно обследовать пациента для того чтобы исключить возможную сопутствующую нестабильность голеностопного сустава, нарушение оси голеностопного сустава – так как они потребуют одновременной коррекции для предотвращения рецидива ОПТК. КТ и МРТ позволяют точно локализовать дефект для того чтобы выбрать правильный хирургический доступ и тактику.
Открытая операция при остеохондральных повреждений таранной кости.
При выполнении доступа к передне-наружному отделу голеностопного сустава необходимо помнить о расположенных в этой зоне ветвях поверхностного малоберцового нерва.
Для доступа к задне-медиальным отделам потребуется выполнить остеотомию медиальной лодыжки, при этом необходимо исключить повреждение плато большеберцовой кости которое несёт основную осевую нагрузку. До выполнения остеотомии необходимо заранее произвести рассверливание для последующей установки фиксирующих остеотомированный фрагмент винтов.
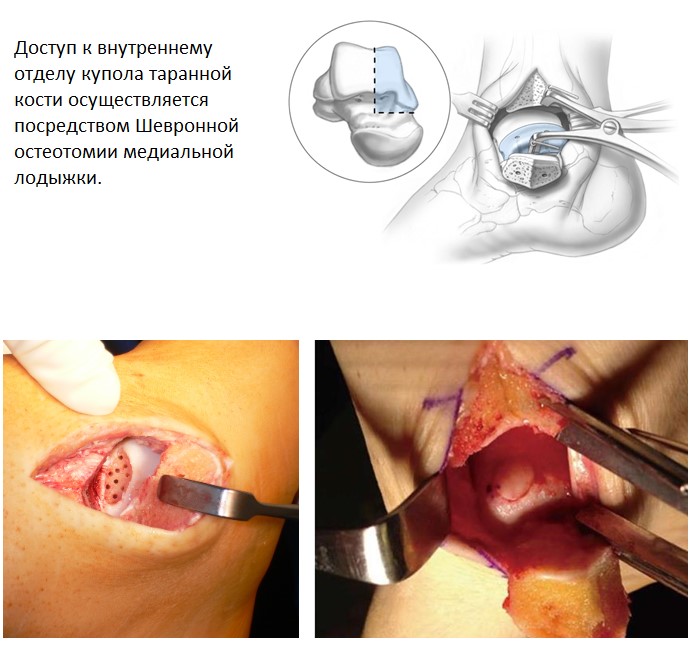
Также следует избегать повреждения переднего и заднего большеберцовых сухожилий, сухожилия длинного сгибателя большого пальца, большой подкожной вены, задней большеберцовой артерии и нерва. Альтернативой является использование сразу двух доступов – антеромедиального и постеромедиального, которые позволяют визуализировать до 80% купола таранной кости и позволяют избежать остеотомии внутренней лодыжки.
В настоящее время широкое распространение получила артроскопия голеностопного сустава. Артроскопические доступы намного менее травматичны, что позволяет избежать формирования грубых послеоперационных рубцов и значительно облегчает реабилитацию. 2,7 мм артроскопы позволяют визуалировать весь купол таранной кости.
Удаление.
Удаление свободного или частично отделённого хрящевого фрагмента. По данным различных исследований эффективность этого метода лечения варьирует от 30 до 88% (в среднем 54%).
Удаление и кюретаж.
После удаления свободного или частично отделённого хрящевого фрагмента производится обработка подлежащей кости и окружающего дефект хряща. Используется для различных дефектов начиная со 2 –й стадии заболевания. Эффективность метода от 56 до 94% (в среднем 77%).
Удаление, кюретаж и стимуляция костного мозга.
После дебридмента производятся несколько каналов сообщающих дефект с костным мозгом. Эту процедуру можно выполнить при помощи рассвуерливания или микрофрактурирования. Целью манипуляции является разрушение барьера из склерозированной суюбхондральной кости препятствующего миграции стволовых клеток из костного мозга. Как результат формируется сгусток насыщенный факторами роста, стволовыми клетками, который в дальнейшем перестраивается в гиалиноподобную хрящевую ткань. Чаще используется для 3-4 стадий заболевания. Размер недекта не должен привышать 1,5 см. В клиническим исследованиях эффективность метода оценивалась от 46 до 100 % (в среднем 85%).
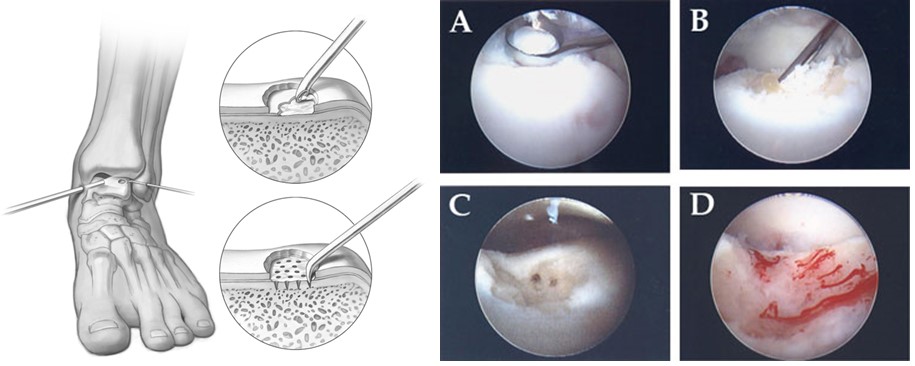
Удаление, кюретаж и аутотрансплантат из губчатой кости.
После дебридмента производится замещение полости аутотрансплантатом из губчатой кости (большеберцовой кости или гребня подвздошной). Данный метод используется для больших дефектов (более 1,5 см2) В клиническим исследованиях эффективность метода оценивалась от 41 до 93 % (в среднем 61%).
Чрезлодыжечное рассверливание.
В случае если дефект расположен глубоко в суставе и доступ к нему при артроскопии ограничен, а артротомию делать не хочется можно использовать методику чрезлодыжечного рассверливания. Для этого Спица Киршнера направляется в сторону дефекта через внутреннюю\наружную лодыжку в зависимости от его локализации под контролем артроскопа. В клиническим исследованиях эффективность метода оценивалась от 32 до 100 % (в среднем 63%).
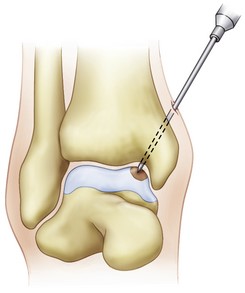
Остеохондральная трансплантация.
Для остеохондральной трансплантации наиболее часто используется хрящевая ткань из ипсилатерального коленного сустава. Показанием для трансплантации являются большие и глубокие дефекты, часто с формированием кисты, а также отсутсвие эффекта от предложенных выше методов хирургического лечения. В настоящее время изучается возможность использования участка пяточной кости в месте ахилло-пяточного сустава как источник ткани для остеохондральной трансплантации в котором получены хорошие ранние результаты.
Задачей метода является восстановление структурных и биомеханических характеристик повреждённого гиалинового хряща. Для данного метода характерен длительный и сложный реабилитационный период. Морбидность донорского места (боли в коленном суставе после забора столбиков костно-хрящевых блоков) наблюдаются в 12% случаев. Сама по себе методика технически сложная и трудоёмкая.
В клиническим исследованиях эффективность метода оценивалась от 74 до 100 % (в среднем 87%).
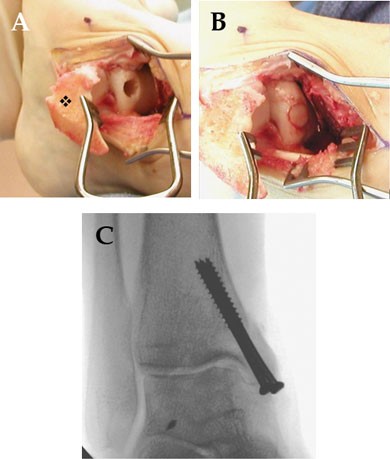
Ретроградное рассверливание.
Для этого метода потребуется использование рентгенологического контроля, и знание точной топографии места расположения дефекта. Ретроградное рассверливание - метод выбора при наличии большой субхондральной кисты и при сохранном суставном хряще а также в случаях глубоко расположения дефекта, когда трудно достичь его при помощи артроскопического метода. Для медиальных дефектов точкой входа спицы становится тарсальный синус. В клиническим исследованиях эффективность метода оценивалась от 81 до 100 % (в среднем 88%).
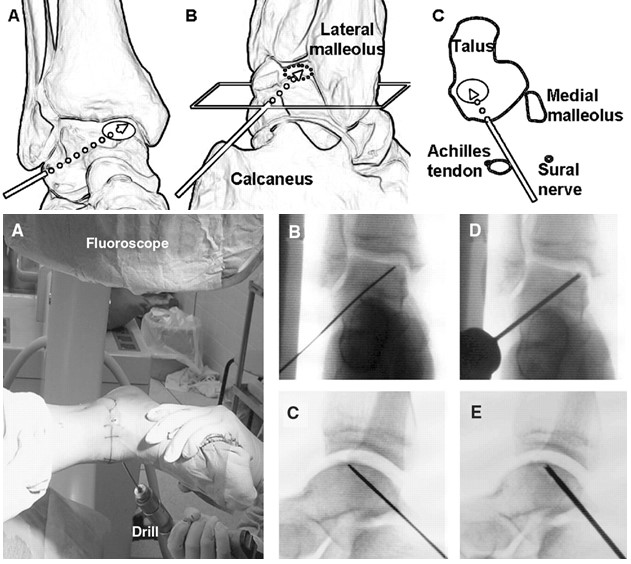
Фиксация.
Фиксация фрагмента производится только в случаях свежих обширных повреждений. Оторванный костно-хрящевой фрагмент приподнимается, подлежащее ложе подвергается микрофрактурированию или рассверливанию, затем фрагмент фиксируется при помощи погружных рассасывающихся винтов или фибринового клея. Метод технически сложный и показания к нему достаточно узкие, однако когда он использовался по показаниям, в 89% случаев наблюдался хороший результат.
Таким образом наиболее эффективным и технически простым методом лечения подавляющего большинства остеохондральным повреждений таранной кости на данный момент является удаление, кюретаж и стимуляция костного мозга. В зависимости от оснащения операционной и навыков оперирующего хирурга данное вмешательство возможно выполинть как открытым способом так и артроскопически.
Реабилитация после операции по поводу остеохондральных повреждений таранной кости.
Большинство авторов придерживается стандартного реабилитационного протокола, рекомендующего 6 недель иммобилизации после оперативного вмешательства с использованием стимуляции костного мозга. Однако в последнее время появляются работы свидетельствующие о том что 2-недельного периода иммобилизации более чем достаточно при малых и средних размерах дефекта. Реабилитация заключается в тренировке активной и пассивной амплитуды движений, мышечной силы и мышечного баланса голени, снижении отёка и проприоцептивной тренировки.
Боли, ощущение заклинивания и отёк часто сохраняются до 1 года после оперативного вмешательства. Через 6 месяцев целесообразно выполнить МРТ контроль для оценки динамики, при наличии выраженного отёка костного мозга прогноз неблагоприятный. В таких случаях прогрессирование поражения может в дальнейшем привести к необходимости выполнения артродеза или протезирования голеностопного сустава.

Автор статьи:
Никифоров Дмитрий Александрович
Хирургия стопы и голеностопного сустава, коррекция деформаций конечностей, эндопротезирование суставов, артроскопическая хирургия, спортивная травма.